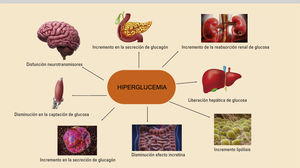
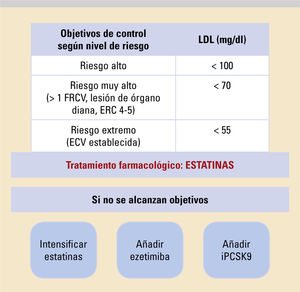
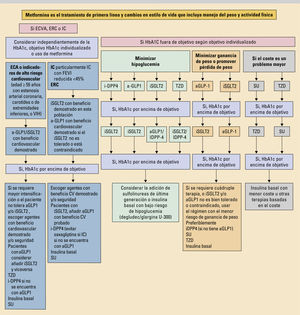
La incidencia actual creciente de la diabetes mellitus tipo 2 (DM2) constituye un verdadero problema de salud pública, y surge la necesidad de mejorar el pronóstico de esta enfermedad. En los últimos años, se ha abandonado progresivamente el enfoque glucocéntrico del tratamiento, para dar paso a un enfoque integral del paciente que permita la individualización del tratamiento, dada la alta heterogeneidad del paciente diabético. En este sentido, son múltiples los aspectos a considerar en la elección del tratamiento (edad, expectativa de vida, preferencias del paciente, etc.). Sin embargo, hoy en día la presencia de enfermedad cardiovascular, enfermedad renal crónica o insuficiencia cardíaca condicionan en gran medida la elección del tratamiento, dados los beneficios cardiovasculares obtenidos con las nuevas familias de fármacos antidiabéticos (agonistas del receptor GLP-1 e inhibidores de sGLT2)
Palabras clave
The rising incidence of type 2 diabetes mellitus (DM2) nowadays represents a true public health problem and there is a need to improve this disease's prognosis. In recent years, a glucocentric treatment approach has progressively been abandoned, giving way to a comprehensive approach to the patient that allows for the individualization of treatment, given the high degree of heterogeneity among diabetic patients. In this regard, multiple aspects must be considered when choosing a treatment (age, life expectancy, patient preferences, etc.). However, nowadays, the presence of cardiovascular disease, chronic kidney disease, or heart failure condition treatment choice to a great extent, given the cardiovascular benefits obtained from new families of antidiabetic drugs (GLP-1 receptor agonists and SGLT2 inhibitors).
Keywords
Identifíquese
¿Aún no es suscriptor de la revista?
Comprar el acceso al artículo
Comprando el artículo el pdf del mismo podrá ser descargado
Teléfono para incidencias
De lunes a viernes de 9h a 18h (GMT+1) excepto los meses de julio y agosto que será de 9 a 15h