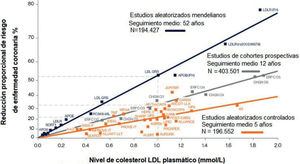
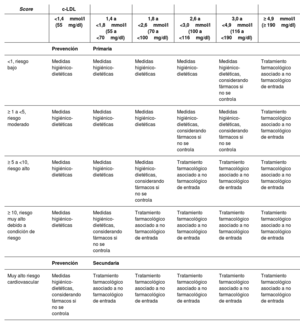
La alteración patológica del metabolismo lipídico (dislipidemia) es una enfermedad muy prevalente que se asocia con la principal causa de mortalidad en el mundo, la enfermedad cardiovascular. El conocimiento de su fisiopatología, su diagnóstico y tratamiento han experimentado cambios en los últimos tiempos que nos permiten alcanzar grados de control hasta hace poco tiempo inimaginables. Tanto la prevención primaria como la secundaria avanzan hacia objetivos cada vez más estrictos, lo que parece asociarse con una disminución de la morbimortalidad causada por la enfermedad cardiovascular. En este texto repasaremos las principales moléculas causantes de la aterogénesis en el organismo humano, así como las principales causas de la dislipidemia y su manejo farmacológico y no farmacológico. Todo ello en el contexto del abordaje de los pacientes en función de su riesgo cardiovascular que, como veremos, es el determinante de los objetivos terapéuticos y de la potencia de la intervención farmacológica que deberemos usar.
Palabras clave
The pathological abnormality of lipid metabolism (dyslipidemia) is a highly prevalent disease associated with the leading cause of mortality in the world, cardiovascular disease. Knowledge of its pathophysiology, diagnosis, and treatment changed in recent times, allowing for reaching levels of control that were unimaginable until recently. Both primary and secondary prevention are moving towards increasingly stringent targets, which seems to be associated with a decrease in morbidity and mortality caused by cardiovascular disease. This text will review the main molecules that cause atherogenesis in the human body as well as the main causes of dyslipidemia and its pharmacological and non-pharmacological management. It is framed in the approach to patients according to their cardiovascular risk which, as shall be seen, is what determines the therapeutic objectives and the potency of the pharmacological intervention to be used.
Keywords
Identifíquese
¿Aún no es suscriptor de la revista?
Comprar el acceso al artículo
Comprando el artículo el pdf del mismo podrá ser descargado
Teléfono para incidencias
De lunes a viernes de 9h a 18h (GMT+1) excepto los meses de julio y agosto que será de 9 a 15h