El asma grave de difícil control o no controlada viene determinada por la imposibilidad de controlar síntomas y exacerbaciones pese a emplear glucocorticoides inhalados en dosis altas y un agonista beta-2 de acción larga el año previo o glucocorticoides orales durante 6 o más meses en el último año sin llegar a controlarse. El primer paso que se debe dar en estos pacientes es descartar otras enfermedades concomitantes, comprobar que cumplen la pauta de tratamiento y diferenciar cuál es su fenotipo (asma T2 alérgica o eosinofílica, o asma no T2) según sus características clínicas y analíticas. En función de dicho fenotipo, se podrá administrar un tratamiento biológico mediante anticuerpos monoclonales anti-IgE (omalizumab), anti-IL-5 (mepolizumab, reslizumab y benralizumab) o anti-IL-4/IL-13 (dupilumab) en los subtipos de asma T2. Para tratar el tipo no T2 puede considerarse la termoplastia endobronquial, los corticoides sistémicos e incluso la azitromicina.
Palabras clave
Severe difficult-to-control or uncontrolled asthma is defined as the impossibility of controlling symptoms and exacerbations despite using high-dose inhaled corticosteroids and a long-acting beta2-agonist in the previous year, or oral glucocorticoids for six months or more of the last year. The first step to take with these patients is to rule out other concomitant diseases, verify their compliance with the indicated treatment, and differentiate which phenotype they have (T2 allergic or eosinophilic asthma or non-T2 asthma) according to their clinical and blood test characteristics. Based on said phenotype, biologic treatment can be administered via anti-IgE (omalizumab), anti-IL-5 (mepolizumab, reslizumab, and benralizumab), or anti-IL-4/IL-13 (dupilumab) monoclonal antibodies in T2 asthma subtypes. To treat non-T2 type asthma, bronchial thermoplasty, systemic glucocorticoids, or even azithromycin can be considered.
Keywords
El asma de difícil control o asma grave no controlada es aquella enfermedad asmática que persiste mal controlada pese a recibir tratamiento con una combinación de glucocorticoides inhalados (GCI) y un beta-2 agonista de larga duración [long-acting beta-2 agonist (LABA)], en dosis elevadas en el último año, o bien glucocorticoides orales durante al menos 6 meses del mismo período1. Se estima que el 5%-10% de los pacientes asmáticos tienen un asma grave y en torno a la mitad de ellos (3%-4%) no están controlados2. Ante estos pacientes, lo primero que se debe hacer es un diagnóstico completo y correcto del asma, revisando que se realice correctamente el tratamiento inhalador ya pautado, y que otras patologías concomitantes estén bajo control. Llegado este punto, lo siguiente será clasificar el asma grave no controlada dependiendo del fenotipo que corresponda en función de la clínica y las pruebas complementarias: asma T2 alérgica (síntomas alérgicos, con IgE específica), asma T2 eosinofílica (rinosinusitis crónica/poliposis nasal, corticodependiente o insensible a glucocorticoides, con eosinofilia en esputo y sangre periférica) o asma no T2 (menor volumen espiratorio forzado en el primer segundo, pacientes fumadores y con mayor atrapamiento aéreo, con predominio de neutrófilos)1.
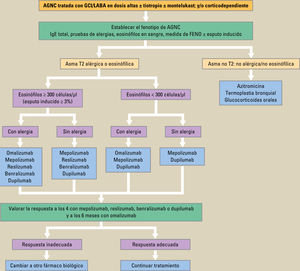
TratamientoExisten distintas opciones terapéuticas aprobadas para tratar este grado de asma según su fenotipo, recogidas en la figura 1, entre las que destacan los fármacos biológicos de reciente introducción en nuestro arsenal terapéutico, salvo omalizumab que ya lleva años en el mercado del asma alérgica.
Tratamiento del asma grave no controlada según el fenotipo inflamatorio.
AGNC: asma grave no controlada; GCI: glucocorticoides inhalados; LABA: agonista beta-2 de larga duración (long-acting beta-2 agonist). Modificada de Guía GEMA 5.11.
Es un anticuerpo monoclonal humanizado que se une a la IgE circulante bloqueando la unión al receptor de alta y baja afinidad (FceR1) para la IgE. Fue el primero en comercializarse hace casi 20 años, demostrando durante este tiempo una mejoría en el volumen espiratorio forzado en el primer segundo (FEV1) en los cuestionarios de calidad de vida, el control sintomático, la reducción de corticoides orales e inhalados, así como de las agudizaciones e ingresos3.
Anticuerpos anti-interleucina 5MepolizumabEs un anticuerpo monoclonal humanizado anti-IgG1 que bloquea la interleucina (IL)-5 circulante y previene su unión al receptor en la superficie del eosinófilo, y que ha demostrado ampliamente una disminución significativa de las exacerbaciones asmáticas y las hospitalizaciones4, una mejoría en la función pulmonar, así como un mejor control clínico y sintomático5.
ReslizumabEs un anticuerpo monoclonal humanizado anti-IgG4K contra la IL-5 que en un estudio con 2 grupos de pacientes redujo las exacerbaciones de modo importante en pacientes con gran eosinofilia en sangre periférica y una o más exacerbaciones en el año anterior en un estudio que comparó este fármaco con placebo, además de incrementar la capacidad respiratoria y la calidad de vida6.
BenralizumabEs un anticuerpo monoclonal humanizado que impide la activación de la IL-5 por medio de la unión a la fracción a de su receptor y promueve la eliminación directa de eosinófilos y basófilos por las células natural killer. Es un fármaco seguro y que reduce la ratio de exacerbaciones anuales e incrementa del valor del FEV1 respecto al previo al tratamiento7.
Anticuerpos anti-interleucina-4/interleucina-13DupilumabEs un anticuerpo monoclonal humanizado contra la subunidad a del receptor de la IL-4 (efecto anti-IL-4 e IL-13), consiguiendo reducir los ingresos por exacerbación asmática en personas con eosinofilia, con mejor función pulmonar y control sintomático8.
AzitromicinaEl uso de azitromicina 500mg vía oral 3 veces a la semana durante 48 semanas reduce las exacerbaciones asmáticas y mejora la calidad de vida en pacientes con asma grave9.
Termoplastia bronquialSe tendrá en cuenta en pacientes que no tengan un fenotipo asmático T2 o en los que los fármacos biológicos no hayan sido útiles, siempre que no haya contraindicaciones y se realice en centros con experiencia en esta técnica1.
Glucocorticoides sistémicosEn algunas situaciones, debido a la imposibilidad de control del asma con otros tratamientos, se deben emplear glucocorticoides orales en la menor dosis y tiempo posible por sus múltiples efectos adversos. La aplicación de triamcinolona depot intramuscular (un glucocorticoide fluorado) puede aportar una significativa reducción de las exacerbaciones, un incremento en la función pulmonar y menos reacciones adversas si se compara con la administración por vía oral1.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
-
 Importante
Importante
-
 Muy importante
Muy importante
-
 Metaanálisis
Metaanálisis
-
 Ensayo clínico controlado
Ensayo clínico controlado
-
 Epidemiología
Epidemiología
-
 Artículo de revisión
Artículo de revisión
-
 Guía de práctica clínica
Guía de práctica clínica