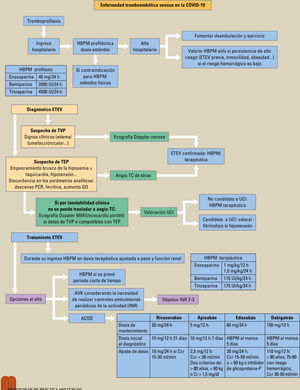
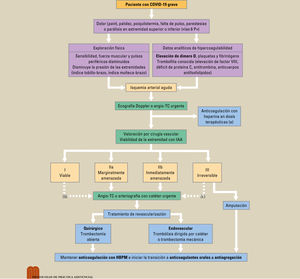
El espectro clínico de la enfermedad producida por el coronavirus SARS-CoV-2 (COVID-19) es muy variable, cursando habitualmente de forma leve o asintomática. En el 15%-20% de los pacientes cursa con afectación pulmonar, que puede evolucionar a síndrome de distrés respiratorio agudo (SDRA) y disfunción multiorgánica, con una marcada alteración en la respuesta inflamatoria e inmunitaria. En estas formas graves, aumenta la prevalencia de complicaciones trombóticas vasculares, manifestadas como tromboembolismo venoso, isquemia arterial aguda en las extremidades y, con menor frecuencia, afectación miocárdica y accidente cerebrovascular. Los mecanismos patogénicos postulados incluyen daño endotelial difuso o endotelitis, inflamación microvascular, liberación de citocinas, hipercoagulabilidad e hipoxia. El reconocimiento temprano de estas complicaciones es vital para mejorar el pronóstico y la supervivencia de estos pacientes.
Palabras clave
The clinical spectrum of the disease caused by SARS-CoV-2 (COVID-19) is highly variable. It commonly has a mild or asymptomatic course. Around 15% to 20% of patients have lung involvement, which can progress to acute respiratory distress syndrome (ARDS) and multiple organ dysfunction syndrome, with marked alteration of the inflammatory and immune response. In these severe forms, there is an increased prevalence of vascular thrombotic complications which manifest as venous thromboembolism, acute arterial ischemia in the limbs, and, less frequently, myocardial involvement or cerebrovascular accident. The proposed pathogenic mechanisms include diffuse endothelial damage or endotheliitis, microvascular inflammation, cytokine release, hypercoagulability, and hypoxia. Early recognition of these complications is vital for improving the prognosis and survival of these patients.
Keywords
Identifíquese
¿Aún no es suscriptor de la revista?
Comprar el acceso al artículo
Comprando el artículo el pdf del mismo podrá ser descargado
Teléfono para incidencias
De lunes a viernes de 9h a 18h (GMT+1) excepto los meses de julio y agosto que será de 9 a 15h